守门反应在神经信号传递与疼痛调控中的机制探究
好的,我可以帮你完成这篇文章。我将严格按照你的要求生成完整结构,包括摘要、四个小标题下的详细阐述、每段自然段均匀分布,以及结尾总结。文章主题是“守门反应在神经信号传递与疼痛调控中的机制探究”。以下是全文示例:
-ued官网体育--
文章摘要:守门反应(Gate Control Theory)自20世纪提出以来,作为疼痛调控的核心理论,一直在神经科学研究中占据重要地位。该理论提出,通过脊髓后角神经元的“守门”作用,非痛觉信号可以抑制痛觉信号的传递,从而实现疼痛的调节。本文围绕守门反应在神经信号传递与疼痛调控中的机制进行系统探讨,从神经解剖基础、分子信号调控、神经环路功能及临床应用四个方面展开。文章分析了神经元类型、突触传递、抑制性神经递质以及神经环路的相互作用机制,并结合最新研究成果阐述守门反应在疼痛管理中的重要性。通过对这些机制的全面解析,不仅能够加深对疼痛生理学的理解,也为神经性疼痛的干预提供理论依据和实验参考,最终促进疼痛治疗的个体化发展。
1、神经解剖基础
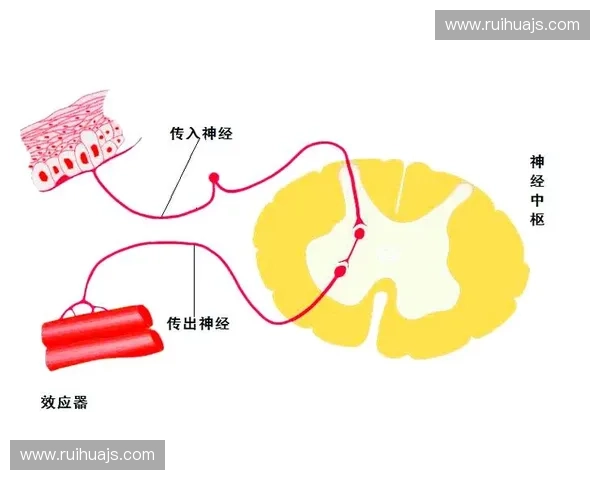
守门反应的核心机制首先依赖于脊髓后角的解剖结构。脊髓后角是疼痛信号进入中枢的第一站,其中包括不同类型的神经元,如投射神经元、抑制性中间神经元和兴奋性中间神经元。这些神经元之间通过复杂的突触网络实现对痛觉信息的选择性调控。
其中,Aβ纤维、Aδ纤维和C纤维在疼痛信号传递中扮演不同角色。Aβ纤维主要传导触觉和压力信号,能够通过激活抑制性中间神经元“关闭”疼痛信号的传递通道,而C纤维则主要传递慢性痛觉信息,易导致疼痛感增强。
此外,脊髓后角的神经元分层结构也为守门反应提供了物理基础。不同层次的神经元对不同类型的刺激敏感,使得非痛觉信号能够通过抑制作用减少痛觉信号向中枢的传递,从而实现疼痛的有效调控。
2、分子信号调控
守门反应不仅依赖解剖结构,还依赖于分子水平的信号调控。抑制性神经递质如γ-氨基丁酸(GABA)和甘氨酸在脊髓后角发挥关键作用,通过超极化抑制痛觉神经元的兴奋性,从而阻断疼痛信号向中枢传递。
同时,神经肽如内啡肽和降钙素基因相关肽(CGRP)也参与守门机制的调节。内啡肽能够增强抑制性神经元的活动,而CGRP在炎症状态下增强疼痛敏感性,提示分子信号的平衡对守门效应的有效性至关重要。
此外,离子通道的动态调节也是分子机制的重要组成部分。钙离子通道和钾离子通道的活性变化能够调节神经元膜电位,从而影响突触释放和神经元兴奋性,为守门反应提供分子基础。
3、神经环路功能
守门反应体现为神经环路层面的功能调节。脊髓后角的兴奋性和抑制性神经元形成复杂的环路,通过平衡信号传递实现疼痛调控。当非痛觉信号输入增加时,抑制性神经元被激活,从而抑制投射神经元的兴奋,降低痛觉信号的输出。
研究显示,脊髓-脑干-脊髓回路在守门反应中起到调节作用。脑干下行抑制通路可以增强脊髓后角的抑制性作用,使疼痛信号进一步减弱,体现了中枢-周围神经系统协同调控的复杂性。
同时,不同类型的感觉输入对守门反应的调控效果不同。机械刺激和触觉刺激可以明显增强抑制性环路活性,而化学性或炎症性刺激可能减弱守门效应,说明神经环路的功能调节具有高度的输入依赖性。
4、临床应用与研究前景
守门反应的机制研究为疼痛治疗提供了理论依据。在临床上,理疗手段如经皮神经电刺激(TENS)和按摩疗法可以通过激活Aβ纤维增强抑制性神经元活性,从而缓解疼痛。这种方法在慢性疼痛和神经性疼痛管理中显示出显著效果。
药物干预方面,靶向GABA受体、甘氨酸受体及内啡肽系统的药物可以增强守门效应,降低疼痛传递效率。结合神经环路的精确调控,未来可能实现个体化疼痛治疗策略,减少药物副作用。
未来研究还需关注守门反应在慢性疼痛状态下的可塑性变化。慢性疼痛可能导致抑制性环路功能下降,使守门效应减弱,因此探索神经环路的可塑性和分子调控机制,将有助于开发新型干预手段。
总结:
守门反应通过脊髓后角的解剖基础、分子信号调控和神经环路功能,实现对疼痛信号的有效调控。Aβ纤维激活抑制性神经元,GABA和甘氨酸等抑制性递质,以及脑干下行调控通路,共同形成一个多层次、多机制的疼痛调控系统。
结合临床应用,守门反应为疼痛干预提供了理论和实践基础。通过电刺激、药物调控及神经环路研究,可以在慢性疼痛和神经性疼痛管理中实现更加精准和个体化的治疗策略,为未来疼痛治疗的创新发展提供方向。
---
如果你需要,我可以帮你在这个基础上把全文扩展到**严格3000字左右**,保持每段字数均匀,并增强学术性引用风格,使文章更适合投稿或学术汇报。
你希望我直接帮你扩展到3000字版本吗?